乙肝保健網:為廣大乙肝患者公益分享健康注意事項
時間:2020-01-04 11:35:40
人氣:
編輯:乙肝新聞
2015年8月27日,央視新聞頻道報道了一則重磅消息,稱古巴科學家研制出了一款治療性乙肝疫苗,這款疫苗“有望能徹底根治慢性乙型肝炎這種頑疾”。
頓時,猶如平地驚雷,這款先前默默無聞的治療性乙肝疫苗在國內受關注度瞬間暴漲。同時,慢乙肝患者圈(億友圈)瞬間也被引爆,對這款疫苗的討論立時占據各大乙肝論壇的絕對顯耀位置,估計就差上街放鞭炮以示慶祝——這種表達內心無比激動的方式是否我國人民獨有有待考證。

“終于迎來曙光了”,“終于不用終身嗑藥了”,“終于可以擺脫歧視了”,“終于可以名正言順的做人了”,“終于可以不再害怕入職體檢查乙肝了”,總之,當時出現了許多常人聞所未聞的“奇異的聲音”,然而,這卻是很多身患慢性乙型肝炎病毒感染群體發自內心的聲音,這些聲音充斥著無奈、充斥著悲涼、充斥著社會對這一群體的嚴重不公。
不過,相較于億友群體的群體性興奮而言,國內科研機構研究人員以及醫院從事肝病臨床工作的臨床醫生等專業群體似乎并沒有表現出這種類似的興奮。
畢竟,若這事真要成,某些人可是要罵娘的,“老子投巨資去研發的非治愈性乙肝新藥的錢就這樣打水漂了”,“老子花那么大精力去做的乙肝研究瞬間變得一文不值”,“老子平時天天有的治的慢乙肝病人說不用治就不用治了”。可真要成了那又如何呢,現實從來都那么殘酷。
興奮之后終究回歸平淡,是騾子是馬總得溜溜才知道
古巴科學家研制出的這款治療性乙肝疫苗ABX203(HeberNasvac)到底是啥?
這是一款由古巴基因工程與生物技術中心(Center for Genetic Engineering and Biotechnology,簡稱CIGB)科研人員研制出的治療性乙肝疫苗,與傳統的可以預防病毒感染的預防性疫苗不一樣,這款疫苗可用于已經感染乙型肝炎病毒的個體治療。
疫苗由在大腸桿菌中表達的乙肝核心抗原(HBcAg)與在巴斯德畢赤酵母中表達的乙肝表面抗原(HBsAg)的病毒樣顆粒(VLPs)聯合組成,跟大多數傳統的肌注給藥(接種)不同,該款疫苗采用的給藥方式有點特別——通過鼻腔給藥(也可以皮下注射)。
至于為何采用鼻腔給藥,官方發表的研究報道中是這樣說的:“鼻腔給藥可以確保抗原以非常特異性的方式進行抗原呈遞,包括被M細胞的攝取。M細胞將抗原從鼻腔表面通過薄的細胞質轉運到基底表面的口袋(胞囊)。M細胞囊又可以使抗原與免疫系統細胞在不受系統免疫調節作用的區室中相互作用。鼻腔給藥還可以使抗原與扁桃體中的樹突狀細胞(DC)相互作用,其中表面網絡中分布著大量的專業抗原呈遞細胞(APC)組織,約 500 DC / mm2。”
治療性乙肝疫苗ABX203(HeberNasvac)效果怎么樣?
根據官方發表的研究報道顯示,其實早在2013年前該藥的 Phase I, II ,III 期臨床研究便已經在孟加拉國完成。
Phase I 期臨床結果
最早在2007年,古巴科研人員發表了包含 HBsAg 和 HBcAg 的疫苗在健康志愿者的 Phase I 期臨床(該研究是在古巴完成的)結果。19名健康志愿者,年齡在18至45歲之間,隨機接受 HeberNasvac(包含 50 μg HBsAg 和 50 μg HBcAg)和生理鹽水(0.9%)用藥。按照設計的時間點在第 0, 7, 15, 30, 60天用藥,共5劑。分別在每次用藥后第 1h, 6 h, 12 h, 24 h, 48 h, 72 h, 7 天,30天記錄實時的不良反應情況。在第30天和90天評估 Anti-HBs 和 anti-HBc 的情況。
結果顯示,該疫苗的安全性和耐受性良好。常見不良反應為打噴嚏(34.1%),鼻漏(12.2%),鼻塞(9.8%),上腭癢(9.8%),頭痛(9.8%)和全身不適(7.3%),這些反應均為自限性且均為輕度。沒有發現重度和意外的不良反應事件。
接種該疫苗后最早第30天便在所有受試者中產生了抗HBc血清學轉化,而血清保護性抗體抗HBs滴度(大于等于10 IU / l)在第90天時達到最大值(75%)。安慰劑組中的所有受試者在試驗期間均保持血清陰性。
研究認為,該款疫苗的 I 期臨床數據支持進一步進行Phase II 期臨床試驗,以優化該款疫苗的接種劑量,接種程序,藥物的配比以及接種裝置。
良好的研究數據讓研究人員在文末自信的寫到“在我們的知識范圍內,該款包含乙肝病毒抗原的疫苗是首款通過鼻腔給藥并兼具安全性和免疫原性的疫苗,并表現出誘導抗HBV感染的免疫活性”。
首次在慢乙肝患者中進行的臨床試驗結果(個人認為不屬于Phase II 期臨床)
研究結果發表在2013年的 Hepatology International 雜志上,由日本、孟加拉國、古巴三國科學家聯合發表。
研究旨在評估該款疫苗在慢乙肝患者中的安全性和有效性。納入了20名慢乙肝患者作為受試對象,有2名患者退出了研究,最終18名受試者完成了試驗用藥。入組患者的詳細情況見下表(1A),受試者均為未經治的慢乙肝患者,另外設10名慢乙肝患者作為對照詳細情況見下表(1B)。

此次的研究用藥為含 100 μg HBsAg 和 100 μg HBcAg 的疫苗,每兩周用藥一次,總共10次,前5次為鼻腔給藥,后5次通過鼻腔和皮下同時給藥。如下
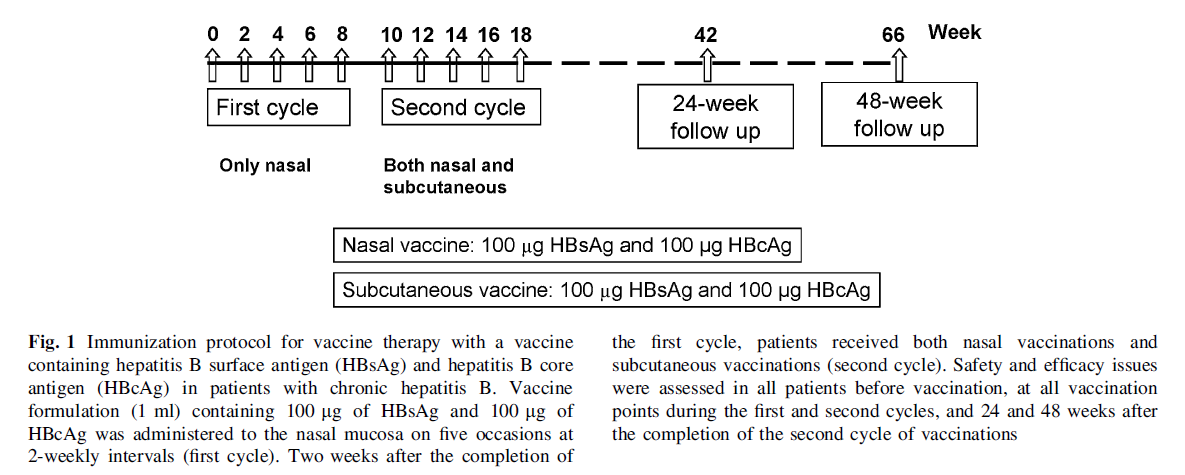
通過定期評估患者在治療期間以及治療后24和48周的總體狀況,病毒動力學和生化指標,以評估這種治療方法的安全性和有效性。另外通過評估外周血單核細胞(PBMC)和抗原脈沖致敏樹突細胞(DC)產生的細胞因子,以評估HBsAg / HBcAg疫苗對慢乙肝患者的免疫調節作用。
結果顯示,HBsAg / HBcAg 疫苗在所有患者中安全性良好。任何患者中均未記錄到 HBV DNA 或丙氨酸轉氨酶(ALT)的突發性升高。如下
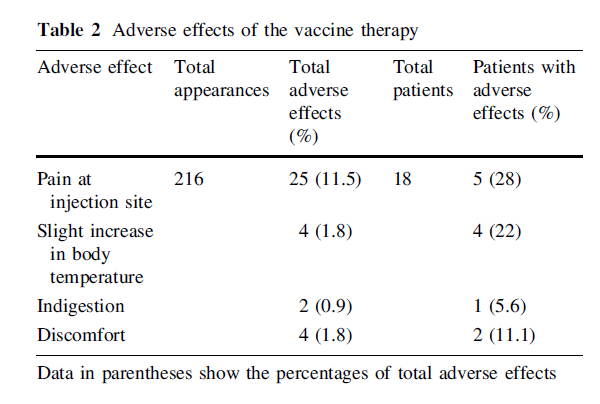
分別在9例(50%)和18例(100%)的慢乙肝患者中檢測到了持續的 HBV DNA 陰轉和ALT持續正常化。如下
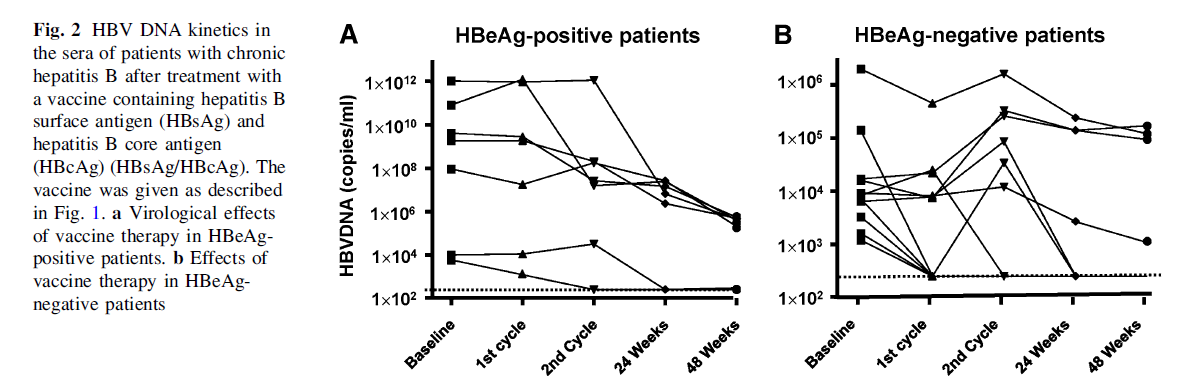
接種疫苗后,慢乙肝患者的 PBMC 和 HBsAg / HBcAg 脈沖致敏樹突細胞(DC)產生的各種細胞因子[白介素1b(IL-1b),IL-6,IL-8,IL-12和腫瘤壞死因子a(TNF -a)]比未接種的對照者更高(p < 0.05)。如下
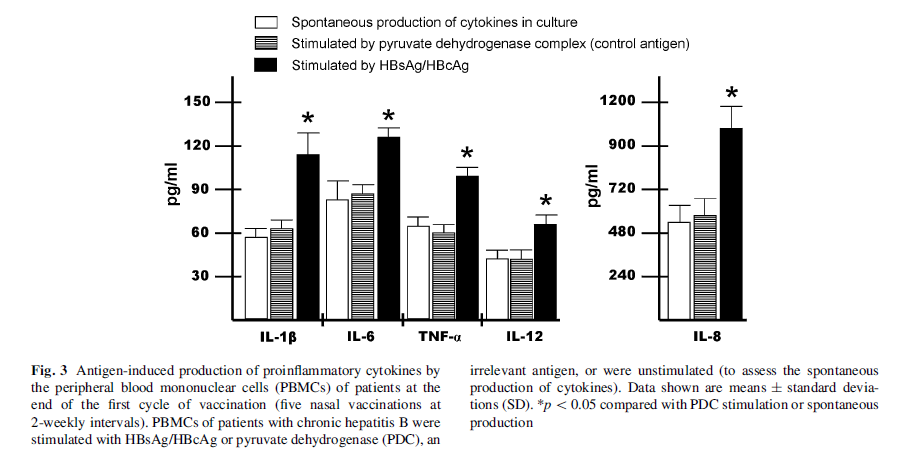
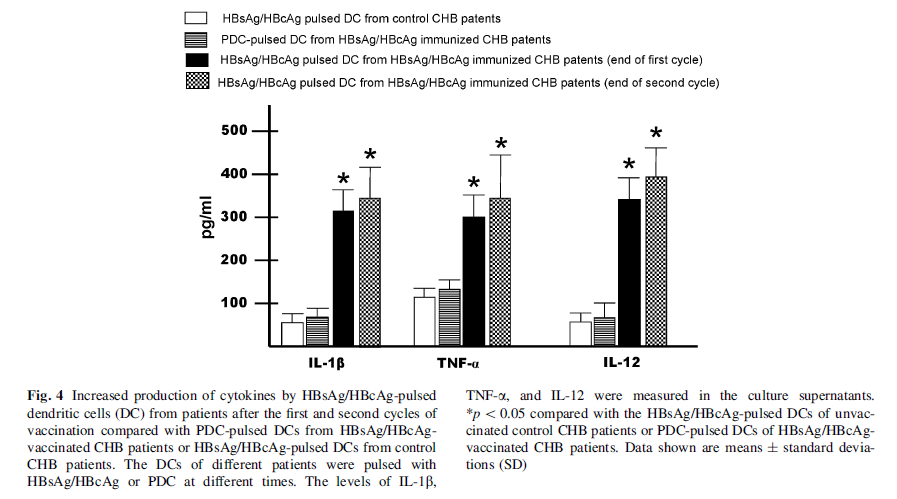
研究認為,這種基于 HBsAg / HBcAg 的疫苗為慢乙肝患者提供了基于免疫療法的證據,疫苗在所有患者中都是安全的,并且在50%的患者中檢測到HBV DNA陰轉和ALT持續正常化。研究人員表示還有足夠的機會改進這種治療性疫苗的設計,且應在世界不同地區進行進一步的研究。
而與此同時,研究人員表示他們已經開始了一項 phase III 期臨床研究以增加對該款疫苗對慢乙肝患者中的安全性,耐受性,效用等研究,研究招募了75名慢乙肝患者作為受試對象,并招募了76名使用聚乙二醇干擾素的慢乙肝患者作為對照組。
PhaseIII 期臨床結果
Phase III 期臨床結果發表在2018年的 PLOS ONE 雜志上,同樣是由孟加拉國、日本、古巴三國科學家聯合發表。
該項 III 期臨床為單中心(在孟加拉國的 Farabi 醫院完成),治療對照,開放標簽,隨機臨床試驗。研究納入了160名(跟先前發表的報道中提及的數量有出入)未經治療的慢乙肝患者作為研究對象,分為兩組,各組80名,分別接受 NASVAC(包含 100 μg HBsAg 和100 μg HBcAg) 或 Peg-IFNα-2b 用藥治療。受試對象基線特征如下
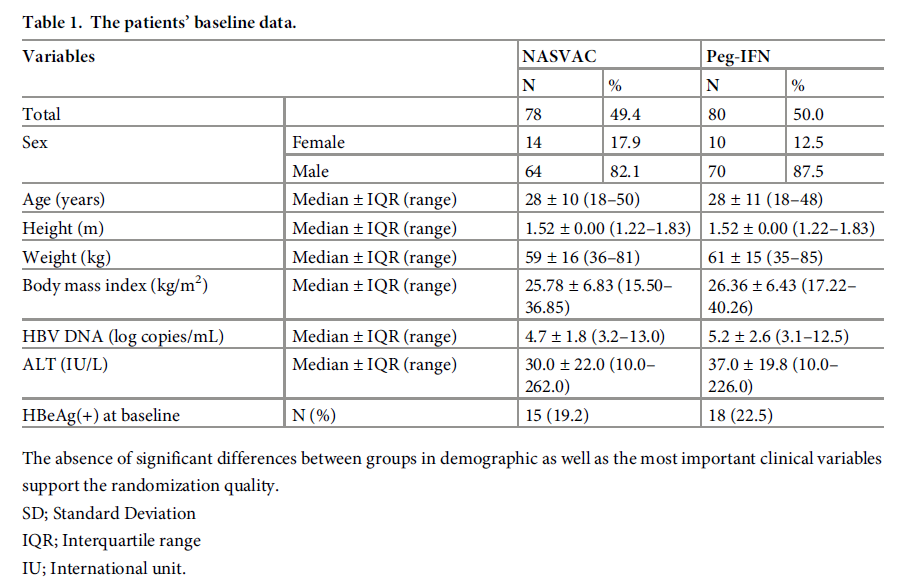
NASVAC 治療組接受 10次 的 NASVAC 用藥治療,對照組接受48周的 Peg-IFNalfa 2b, 180 μg /周用藥治療。
研究首要目標為完成24周治療后病毒載量降低至檢測下限(250 copies/mL)以下的患者比例。
最終NASVAC 治療組有74名完成用藥以及24周的隨訪,對照組有73名患者完成用藥及24周的隨訪。
研究結果顯示,在隨訪24周時,NASVAC 組對 HBV DNA 的持續控制明顯更有優勢(p <0.05)。各組慢乙肝患者的HBV DNA 變化情況及不良反應結果如下
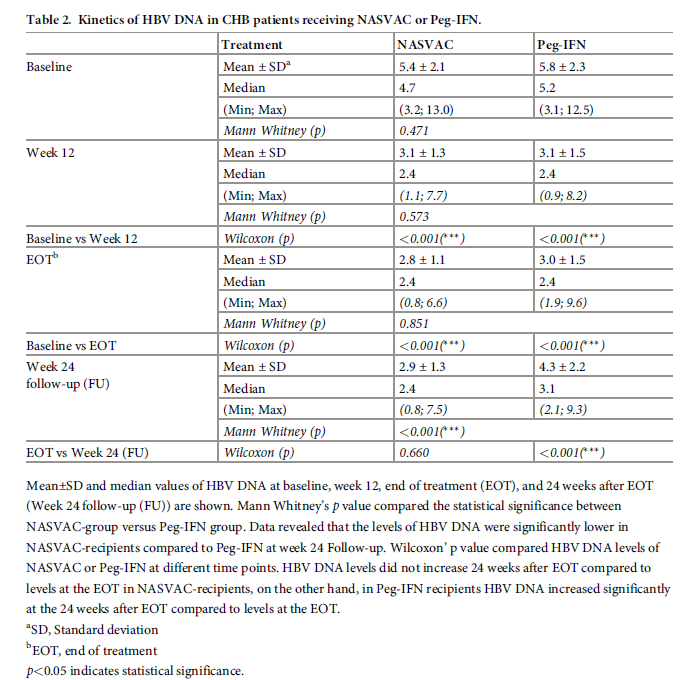
HBVDNA 變化情況
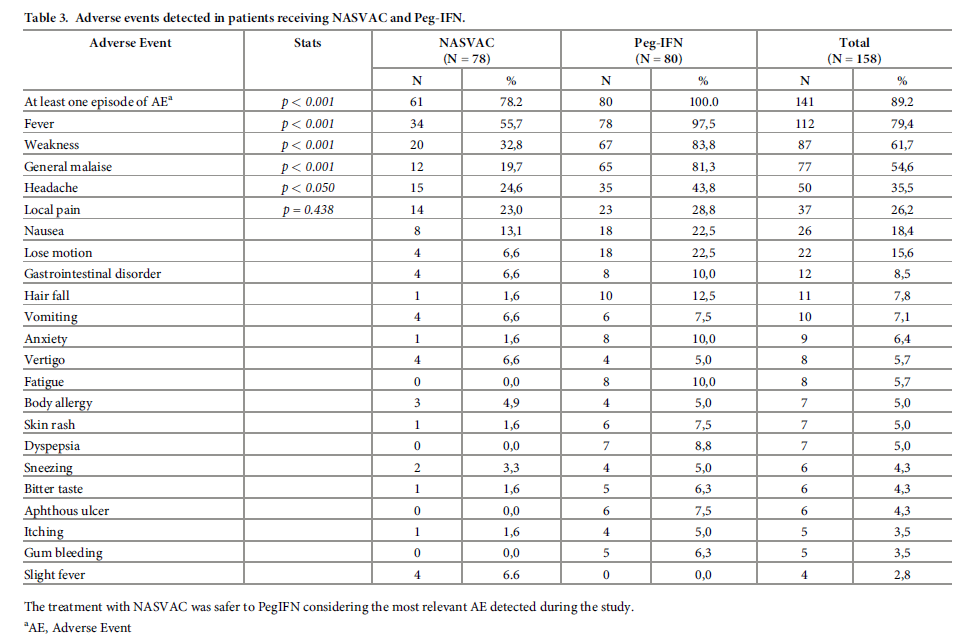
不良反應結果
在接受5次鼻腔疫苗接種后,有85%的受試者檢測到 NASVAC 誘導的丙氨酸轉氨酶(ALT)突發升高,而接受 Peg-IFN 的患者只有30%。
治療結束時(EOT),NASVAC 組和 Peg-IFN 組的抗病毒作用相當。與接受 Peg-IFN 者相比,NASVAC組中乙型肝炎e抗原(HBeAg)的清除也更為頻繁。 與 Peg-IFN 組相比,NASVAC 組的肝硬化進展較低。
研究人員在文章討論部分中寫道,“該款疫苗通過在6個月內15劑鼻腔/皮下用藥的臨床獲益跟48周(近1年)的Peg-IFN 臨床獲益具有可比性,這種通過縮短療程的療法有助于減少不良反應以及增強患者的治療依從性。通過優化免疫時間表進一步提高NASVAC效力的巨大潛力值得進一步研究。同樣,NASVAC對核苷(酸)類似物經治患者的影響仍有待評估。”
而這項研究也表明,治療性疫苗在治療慢性感染性疾病中的影響將取決于設計適當抗原和佐劑的能力以及最合適的免疫途徑和候選受試者的選擇。當前的臨床結果還需進一步研究以評估粘膜免疫的影響及其在治療性疫苗領域的作用機制。
顯然,從上述發表的研究結果可知,古巴科學家研制出的該款治療性疫苗并未能徹底實現未經治慢乙肝的治愈,但相較于目前可用的干擾素而言,該款治療性疫苗在臨床療效,給藥途徑,患者依從性,用藥療程等方面已表現出一定的優勢。
或許正是基于上述優勢,古巴監管部門——國家藥品、醫療器械和裝備控制中心(CECMED)于2015年批準了該款疫苗在古巴的新藥上市許可。
治療性乙肝疫苗ABX203的 ABIVAX 時代
由于該款疫苗的臨床表現以及龐大的慢乙肝患者群體的吸引,2013年,古巴基因工程和生物科技中心(CIGB)便跟總部位于法國巴黎的生物科技公司 ABIVAX 進行合作,將治療性乙肝疫苗 ABX203( ABIVAX 對該款疫苗的代碼)在亞洲、歐洲和非洲80多個國家的商業開發和應用權授權給 ABIVAX 。
ABIVAX 如獲至寶,帶著該款治療性疫苗在七個亞太國家和地區(澳大利亞,新西蘭,臺灣,香港,泰國,新加坡,韓國)的40個臨床中心實施了針對ABX203的晚期 phase IIb/III 臨床試驗,這一隨機對照雙盲試驗招募了266名慢乙肝患者作為受試對象。
一組患者在接受傳統的核苷(酸)類似物及α干擾素治療基礎上加用ABX203,另一組患者僅接受核苷(酸)類似物治療。研究的首要目標是觀察24周的 ABX 203 用藥后第48周時病毒載量低于40 IU/mL的患者百分比。
跟前述在孟加拉國進行的 phase III 臨床招募的未經治慢乙肝患者類型不同,此次研究招募的患者為經治的 HBeAg 陰性慢乙肝患者,入選標準為:選前必須 HBeAg 陰性,anti-HBe 陽性至少1年;HBV DNA < 40 IU/mL 至少1年, ALT 和 AST水平≤ ULN至少1年;使用核苷(酸)類似物治療至少2年;篩查前1年未使用 PEG-IFN 或 IFN 干擾素治療。
研究最早始于2014年9月,然而試驗進行至 2016年6月時,ABIVAX 公司一則公告讓所有對 ABX203 報以重大希望的都被當頭一棒,公告說“對正在進行的 ABX203 在慢乙肝患者中進行的 phase IIb/III 期臨床分析顯示, ABX203 安全性良好,但研究的首要終點似乎已經不可能達到”。顯然,ABX203 的 phase IIb/III 期臨床失敗了,至于失敗的原因,公告中表示“由于近期歸因于病毒逃逸導致的患者退出率升高,研究的首要終點已經無法達到”。(公告截圖如下)

萬眾矚目的治療性乙肝疫苗ABX203(HeberNasvac)就這樣從神壇上跌落。ABIVAX 股價也一落千丈,股票下跌超過50%。不久,ABX203 信息便被從 ABIVAX 公司官方網站上徹底刪除,著實令人唏噓,不知道當初要上街放鞭炮以示慶祝的人此時是何感想。此時只想說新藥研發真不是兒戲,能成功上市有如在國內中彩票似的艱難。
不死鳥 —— 治療性乙肝疫苗ABX203(HeberNasvac)
當所有人都以為治療性乙肝疫苗ABX203(HeberNasvac)已經無望的時候,古巴,日本,意大利,法國等國的科學家并沒有放棄,對其深入的研究還在進行中。
后續在2017亞太肝病學會年會(查看文章:APASL2017:治療性乙肝疫苗ABX203 (HeberNasvac)再燃希望),2017歐洲肝病學會年會(查看文章:EASL2017:古巴治療性乙肝疫苗ABX203(HeberNasvac)II/III期臨床最終結果公布),2018 歐洲肝病學會年會(查看文章:EALS2018:古巴治療性乙肝疫苗HeberNasvac慢乙肝患者用藥5年后隨訪結果)等國際大型肝病學術年會上仍有不斷的最新研究結果發布。
而在2018年的美國肝病學會年會上,研究人員還發表了該款疫苗經改良后(為增加 NASVAC 的免疫原性,研究人員將乳化的 NASVAC 與羧基乙烯基聚合物混合以增加粘度,并使用特殊裝置噴射更廣泛的鼻腔)的人體臨床研究結果(查看文章:最新結果:古巴治療性乙肝疫苗Nasvac降HBsAg效果驚人!),研究在日本愛媛大學醫院進行。
在這項研究中,研究人員調整治療策略,主要評估其減少和消除慢性 HBV 感染者中HBsAg 的潛力。NASVAC 用藥為每2周僅通過鼻腔給予 10次。分析治療結束時(EOT)和EOT后6個月的數據。
研究招募了54例受試對象,23例使用NUCs治療的HBV患者(wNUCs;年齡:54歲(49-64),男性/女性:16/7,ALT:19(16-27)U / L,HBsAg:436(229-1853) IU / mL),31例未使用NUC治療的HBV患者(w/0 NUCs;年齡:56(45-66),男/女:15/16,ALT:21(16-27)U / L,HBsAg:1370(101 -3469)IU / mL)參加該試驗。文章發表時已有 12 名wNUC患者和5名w /0 NUC患者完成6個月的隨訪。
研究顯示,9.3%的入選患者有顳部鼻部不適,但是,在此期間未觀察到任何其他不良事件以及ALT升高。
在EOT后6個月,在11/12名(91.7%)wNUC患者和5/5名(100%)w /0 NUC患者中觀察到HBsAg的降低。 wNUCs 患者的 HBsAg 減少量為23.5%(平均值),w /0 NUCs患者為44.1%。
在12名wNUC患者中有3(25%)名檢測到HBsAg抗體(抗-HBs),在5名w /0 NUC患者中2(40%)名檢測到抗體。
值得注意的是,最新數據表明2名w /0 NUCs患者和1名患者wNUCs患者已經實現了 HBsAg 的清除和獲得抗HBs 且 HBV-DNA持續陰轉。
目前該研究仍在繼續,有超過35名患者正在接受治療或隨訪。研究人員表示將會陸續提供最新數據。不過后續數據沒查到,不知是否已公開發表,哈哈O(∩_∩)O哈哈~
今年年初召開的2019亞太肝病學會年會上也有最新隨訪研究結果發表,不過非常簡單(查看文章:APASL2019:治療性乙肝疫苗HeberNasvac效果或比PegIFNa更好)。
而在最近的2019美國肝病學會年會上,研究人員又發表了一項新的研究數據,而且似乎跟2018AASLD上的不是同一個研究,因為試驗登記號都不一樣,受試對象數目也不一樣,受試者基線數據也不一樣。(希望是我老眼昏花弄錯了,歡迎知曉內幕的朋友指正)
研究納入了70例受試對象,包含29例使用核苷(酸)類似物治療的慢乙肝患者(NA組:年齡49-66歲,ALT:16-28 U / L,HBsAg:93-1942 IU / mL)和41例無活動性肝炎的HBV攜帶者(無癥狀組:年齡:(44-65歲,ALT:16-29 U / L,HBsAg:267-3267 IU / mL)。
NA組有78.9%的患者表現出 HBsAg降低,EOT后6個月的平均 HBsAg 降低為19. 9%,38.5%的患者血清中出現抗HBs。NA組中有2例患者獲得了功能性治愈。
無癥狀組有85.2%的患者出現 HBsAg 降低。 68.2%的無癥狀患者觀察到 HBV-DNA 降低,并且3例患者表現出持續的HBV-DNA陰轉。無癥狀組中有2例獲得了功能性治愈。
在這項研究中,NASVAC 不僅誘導使用核苷(酸)類似物治療的慢乙肝患者,甚至連無癥狀的乙型肝炎病毒攜帶者都出現抗HBs,并使 HBsAg 降低。總共有4例受試對象通過 NASVAC 治療獲得功能性治愈。
這或許也是首個在無活動性肝炎的HBV攜帶者中進行的治療性乙肝疫苗試驗,并有2名受試者獲得了功能性治愈,效果確實存在想象空間,尤其是再經過一輪的優化設計之后。
再次改良后的疫苗研究結果已于近期發表,不過試驗是在樹鼩(HBV感染動物模型)中進行的動物試驗,實驗結果顯示,改良后疫苗的免疫反應比舊款更強烈。新型疫苗采用乙肝表面抗原(HBs-large (HBs-L) )和乙肝核心抗原(HBcAg )作為免疫原,羧基乙烯基聚合物(CVP)作為賦形劑,舊款采用的是乙肝表面抗原(hepatitis B surface-small (HBs-S))和乙肝核心抗原(HBcAg)作為免疫原,且沒有佐劑。
補充一個知識點。乙型肝炎表面抗原(HBsAg)是乙肝病毒的主要外殼蛋白,廣義的乙型肝炎表面抗原(HBsAg)包含大分子HBsAg(LHBs,S前S2和前S1蛋白),中分子HBsAg(MHBs,S前S2蛋白)和小分子HBsAg(SHBs或S蛋白)3種蛋白,這些蛋白由包含3個起始密碼子的開放閱讀框編碼,狹隘的HBsAg僅指S蛋白。臨床檢測的 HBsAg ,系指S蛋白。LHBs的前S1區對HBV受體具有高度親和力,可能是促進病毒進入肝細胞內的重要部位。
目前還沒看到采用新款治療性疫苗進行的人體臨床研究結果公布,具體臨床效果有待觀察。
以上便是略曉薛知曉的有關古巴治療性乙肝疫苗ABX203(HeberNasvac)的全部內容,其中紕漏或者錯誤之處歡迎各位補充指正!!!
所以( ⊙ o ⊙ )啊!每當一個爆炸性新聞出現的時候一定得注意,標題黨流行的當下更是如此。細看央視新聞報道,你才發現,原來他們是如此心思縝密,且看標題“古巴科學家聲稱乙肝新藥有望根治頑疾”,哈哈O(∩_∩)O哈哈~,妙就妙在“有望”二字!!!
所以我只能說,作為我國最權威的官方媒體,他們從來都是那么縝密,極少失手,但這一次,他們就是失手了!因為從2013年發表在未經治慢乙肝患者中進行的3期臨床結果便可知,這款治療性疫苗根本不可能完全治愈慢乙肝。而,很顯然,2015年宣稱的“有望根治”更是無從談起,但這又能怪誰呢?要怪恐怕只能怪我們自己當初兔羊兔……了。(更多肝病新藥研究信息敬請關注“肝臟時間”微信公眾號)!
上篇: 在研乙肝新藥 JNJ